طاقة التأين الثاني للصوديوم

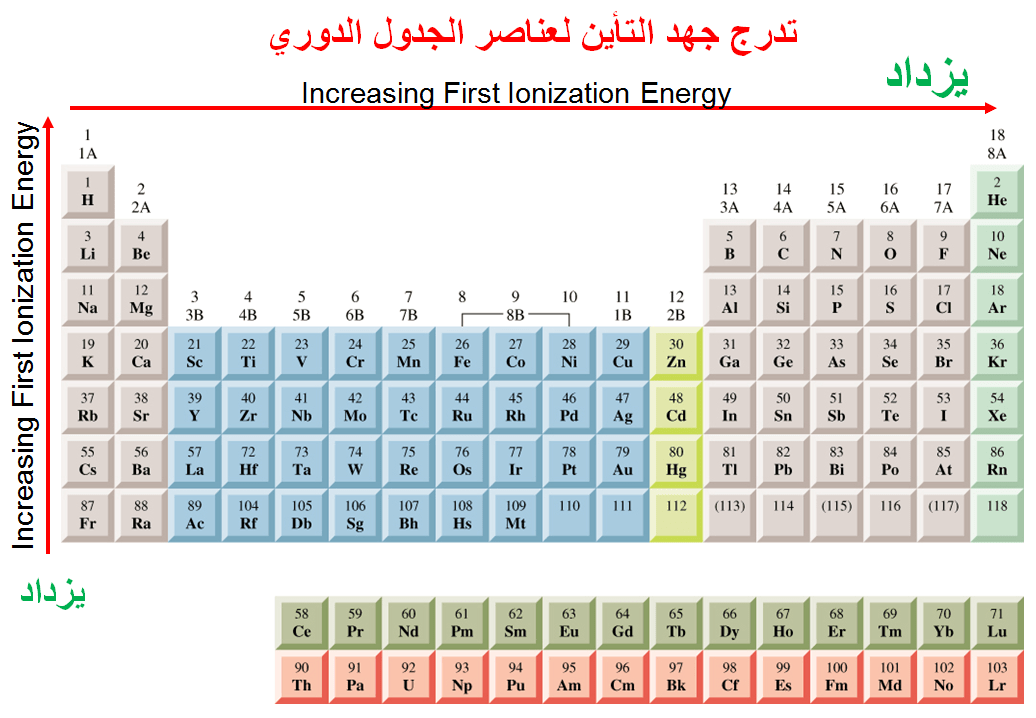
طاقة التأين هي الطاقة اللازمة لإزالة إلكترون من ذرة أو أيون في الحالة الغازية. يزداد طاقة التأين بشكل عام مع زيادة العدد الذري للعنصر، ومع إزالة كل إلكترون، تزداد طاقة التأين.
{ |}
|}
طاقة التأين الأول للصوديوم

طاقة التأين الأول للصوديوم هي الطاقة اللازمة لإزالة إلكترون من ذرة الصوديوم في حالتها الأساسية. يمتلك الصوديوم إلكترون تكافؤ واحد في مداره الخارجي، ويمثل طاقة التأين الأول عملية إزالة هذا الإلكترون. يتم التعبير عن معادلة طاقة التأين الأول للصوديوم على النحو التالي:


Na(g) → Na+(g) + e–

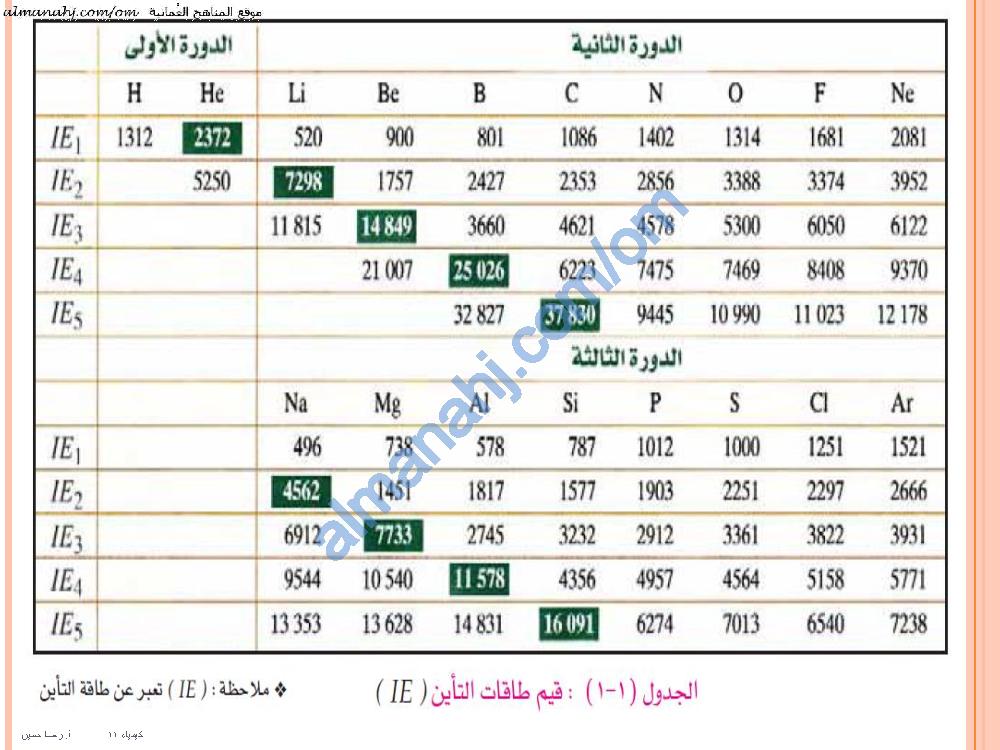
تبلغ قيمة طاقة التأين الأول للصوديوم 496 كيلو جول / مول.
طاقة التأين الثاني للصوديوم

طاقة التأين الثاني للصوديوم هي الطاقة اللازمة لإزالة إلكترون من أيون الصوديوم أحادي الشحنة في حالته الأساسية. بعد إزالة الإلكترون الأول، يصبح أيون الصوديوم أكثر استقرارًا بسبب فقدان الإلكترون الخارجي وتكوين توزيع إلكتروني للغاز النبيل. لذلك، تتطلب إزالة الإلكترون الثاني طاقة أعلى بكثير من طاقة التأين الأول. يتم التعبير عن معادلة طاقة التأين الثاني للصوديوم على النحو التالي:
Na+(g) → Na2+(g) + e–
{|}
تبلغ قيمة طاقة التأين الثاني للصوديوم 4562 كيلو جول / مول.

لماذا طاقة التأين الثاني للصوديوم أكبر من طاقة التأين الأول؟
{ |}
|}
هناك عدة أسباب لكون طاقة التأين الثاني للصوديوم أكبر بكثير من طاقة التأين الأول:

* شحنة النواة الفعالة: بعد إزالة الإلكترون الأول، يصبح أيون الصوديوم أحادي الشحنة موجبًا. يؤدي ذلك إلى زيادة الشحنة النووية الفعالة التي يشعر بها الإلكترونات المتبقية، مما يجعل من الصعب إزالة الإلكترون الثاني.

* حجم الأيون: بعد إزالة الإلكترون الأول، يتقلص حجم أيون الصوديوم. يؤدي هذا إلى تقليل المسافة بين النواة والإلكترونات المتبقية، مما يزيد من قوة التجاذب الكهروستاتيكي بينهما ويجعل من الصعب إزالة الإلكترون الثاني.

* توزيع الإلكترون: بعد إزالة الإلكترون الأول، يتغير توزيع الإلكترون في أيون الصوديوم. يصبح التوزيع أقل استقرارًا، مما يزيد من الطاقة اللازمة لإزالة الإلكترون الثاني.
استنتاج

طاقة التأين الثاني للصوديوم أكبر بكثير من طاقة التأين الأول بسبب زيادة الشحنة النووية الفعالة، وتقليل حجم الأيون، وتغيير توزيع الإلكترون. هذا يجعل من الصعب إزالة الإلكترون الثاني من أيون الصوديوم مقارنةً بإزالة الإلكترون الأول من ذرة الصوديوم.
